Vaccinul anti-HIV care ar putea schimba totul. Primele teste pe oameni dau rezultate uimitoare!
O nouă abordare a vaccinului împotriva HIV arată promisiuni timpurii.
European Medicine Agency a publicat o clarificare privind vaccinul Comirnaty, produs de Pfizer-BioNtech. referindu-se la doza de rapel, EMA a specificat care este intervalul la care trebuie...
Comitetul pentru Medicamente Umane (CHMP) al European Medicines Agency (EMA) a actualizat informațiile despre produs pentru vaccinul COVID-19 Comirnaty pentru a clarifica poziția sa asupra intervalului dintre prima și a doua doză.
Informațiile despre produs (secțiunea 4.2 și prospect) recomandă acum administrarea celei de-a doua doze la 3 săptămâni după prima doză, adică 21 de zile, nu mai mult. Anterior, informațiile despre produs indicau că intervalul ar trebui să fie „cel puțin 21 de zile”.
Informațiile despre produs (secțiunea 5.1) afirmă deja că participanții ale căror date au fost utilizate pentru a calcula eficacitatea au primit a doua doză în termen de 19 până la 42 de zile de la prima doză. A fost adăugată o propoziție cu informația că 93,1% dintre acești participanți au primit a doua doză la 19 până la 23 de zile după prima doză.
În prezent, nu există date clinice privind eficacitatea vaccinului atunci când este administrat dincolo de intervalele utilizate în studiul clinic.
Informațiile complete pentru pacienți și profesioniștii din domeniul sănătății sunt disponibile în informațiile actualizate despre produs.
Comirnaty este un vaccin pentru prevenirea bolii coronavirus 2019 (COVID-19) la persoanele cu vârsta de 16 ani și peste.
Conține o moleculă numită ARN mesager (ARNm) cu instrucțiuni pentru producerea unei proteine din SARS-CoV-2, virusul care provoacă COVID-19. Vaccinul funcționează pregătind corpul să atace proteina spike de pe suprafața SARS-CoV-2.
Informațiile despre produs pentru Comirnaty au fost actualizate într-o variantă de tip IB. Revizuirea a fost efectuată de Comitetul pentru produse medicamentoase de uz uman (CHMP), responsabil pentru întrebările referitoare la medicamentele de uz uman, care a adoptat avizul agenției. Avizul CHMP este urmat imediat de o decizie finală obligatorie din punct de vedere juridic a Comisiei Europene aplicabilă în toate statele membre ale UE.
O nouă abordare a vaccinului împotriva HIV arată promisiuni timpurii.
Vaccinul anti-COVID produce efecte și după ani de zile. Ce s-a aflat abia acum.
Adrian Streinu-Cercel anunta ca în noul cadru legislativ vaccinarea va fi obligatorie pentru toți medicii de familie.
Acest tratament reduce semnificativ inflamația din organism. Poate fi folosit în tratarea cancerului și a COVID.
Milioane de oameni cred că vaccinul COVID nu este un vaccin real. Care e adevărul, de fapt?
Moderna retrage cererea pentru vaccinul combinat antigripal COVID.
Ce este, de fapt, polivaccinarea. Cum se face și care sunt avantajele.
Un nou studiu confirmă. Care este legătura între vaccinurile COVID și riscul de convulsii.
Comisia Europeană a autorizat vaccinul actualizat COVID-19 de la Novavax, conceput special pentru a viza tulpina JN.1 a COVID.
Vaccinul pneumococic polizaharidic cu 23 de valenţe a fost inclus pe lista medicamentelor gratuite.
Acesta este efectul pe care vaccinul anti-COVID îl are asupra organismului. Efectele se vor resimți pe termen lung.
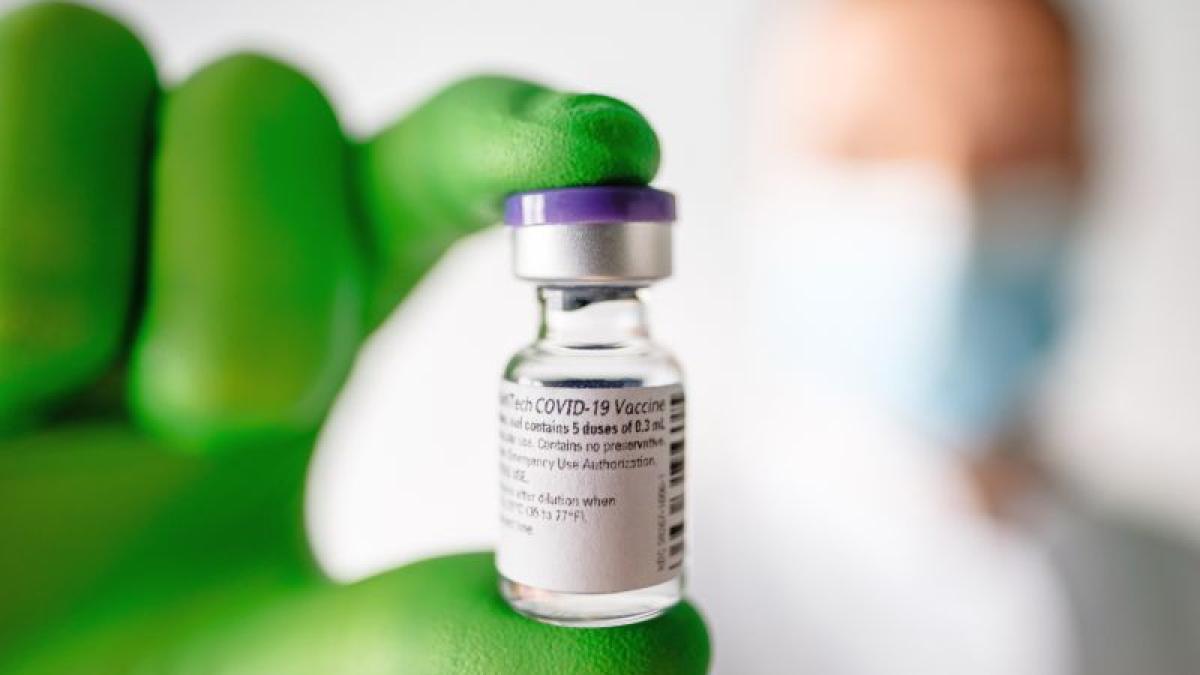 Vaccinul produs de Pfizer și BioNTech. Foto: BioNTech
Vaccinul produs de Pfizer și BioNTech. Foto: BioNTech